La nutrición mineral (Parte 1ª)
Por Víctor Bataller (TRABE)
De todos los nutrientes minerales presentes en las plantas los que representan más del 90% de su peso seco son el carbono, oxígeno e hidrógeno y el resto corresponde a otros elementos cuya presencia es fundamental para un correcto desarrollo. Los toman en forma de iones inorgánicos disueltos en el agua que la planta absorbe por las raíces o bien en los gases que se intercambian por los estomas de las hojas con el medio exterior, CO2 y O2 principalmente.
Según sus concentraciones en la planta los nutrientes se clasifican en dos grupos:
– macronutrientes: son los que se encuentran en cantidades elevadas dado que las necesidades de la planta para cada uno de ellos son muy altas. Son nitrógeno, fósforo, potasio, magnesio, calcio y azufre.
– micronutrientes: se encuentran en cantidades menores aunque son tan importantes como los macronutrientes. Es el caso del hierro, cobre, cinc, molibdeno, manganeso, boro y cloro.
Todos ellos son nutrientes esenciales dado que tienen una influencia directa sobre el metabolismo de la planta, siendo su presencia fundamental para la completar el ciclo biológico y no se pueden reemplazar por otros. Para poder ver la importancia de ésta afirmación vamos a verlos uno por uno.
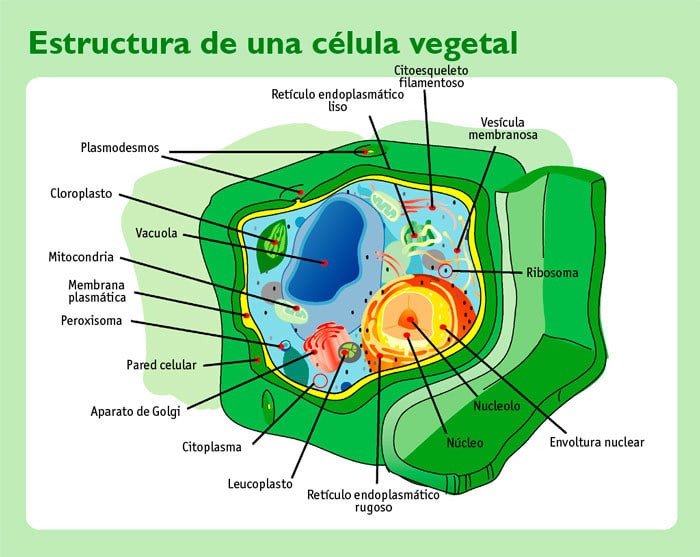
CARBONO
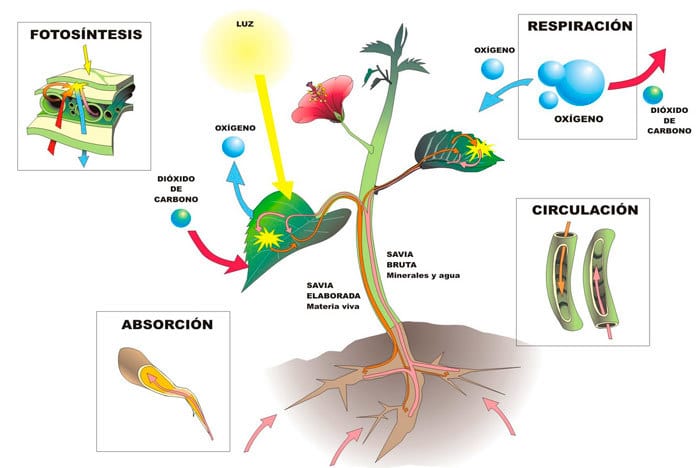
Absorbido principalmente por la planta en forma de dióxido de carbono (CO2). Constituye aproximadamente el 44% del peso seco total de la planta dado que es la base fundamental para la formación de compuestos orgánicos. Es el elemento al que se unen el resto de nutrientes esenciales constituyendo la base estructural de las cadenas de todas las moléculas orgánicas. El CO2 junto con el agua y la aportación de energía de la luz solar participa en el proceso de la fotosíntesis, formando hidratos de carbono que son la fuente de energía tanto del reino vegetal como del reino animal.
OXÍGENO
Tomado por la planta principalmente en forma agua (H2 O) u oxígeno atmosférico (O2) y constituye otro 44% del peso seco total de la planta. Su papel el mismo que el del carbono, forma parte esencial en la estructura molecular de los compuestos orgánicos y además facilita la formación de macromoléculas. El oxígeno forma parte esencial en el proceso de respiración de las plantas porque interviene en la rotura de enlaces de las cadenas de los hidratos de carbono para la obtención de energía.
HIDRÓGENO
Tomado exclusivamente en forma de agua. Forma el 6% del peso seco total de la planta y es un componente fundamental en muchas sustancias orgánicas, desde los aminoácidos hasta los glúcidos.
Una de las aportaciones más importantes desde el punto de vista biológico del hidrógeno es la formación de los Enlaces por Puentes de Hidrógeno. Consiste en un átomo de hidrógeno unido a un átomo relativamente electronegativo que dona el otro hidrógeno al enlace. Los átomos electronegativos suelen ser el flúor, el oxígeno y el nitrógeno. El carbono también puede participar en enlaces de hidrógeno siempre y cuando esté unido a otros átomos electronegativos. Los enlaces por puentes de hidrógeno aparecen en la formación de las estructuras físicas del agua, siendo los responsables de sus distintos estados (sólido, líquido y gaseoso). También son fundamentales en las estructuras de muchas proteínas y del ADN.
NITRÓGENO
Absorbido por la planta como NO3– o NH4+. Es el compuesto básico para la fabricación de aminoácidos, proteínas, nucleótidos, ácidos nucleicos, clorofila y coenzimas. Sus concentraciones son muy variables ya que pueden ir del 1 al 4%. En el abonado nitrogenado es muy importante conocer en qué forma se nos presenta el nitrógeno pues cada una de ellas va a seguir un proceso de transformación diferente hasta alcanzar la forma de asimilación correcta. A la hora de adquirir un formulado se nos debe informar si se encuentra en forma mineral u orgánica.
En forma mineral es el alimento básico de la planta pero éste puede provenir de una base orgánica o de síntesis. Si es de origen orgánico el nitrógeno se acumula en el suelo bajo forma de humus orgánico, luego es mineralizado muy lenta y progresivamente por bacterias para convertirse finalmente en nitrógeno nítrico. Los formulados minerales de síntesis además de presentarse el nitrógeno en forma de nítrico también pueden presentarse en otras dos formas:
El nitrógeno ureico es una forma no asimilable directamente por la planta. En condiciones de humedad, temperatura y mediante la enzima ureasa se transforma rápidamente en nitrógeno amoniacal.
El nitrógeno amoniacal es el resultado de la primera transformación del nitrógeno orgánico. Esta forma del nitrógeno es soluble en agua y queda retenido por el poder absorbente del suelo. Es una forma transitoria, que se transforma en nitrógeno nítrico. Este proceso consta de dos partes, la nitritación, el amoniaco es oxidado a nitrito por unas bacterias y la nitratación, los nitritos son oxidados a nitratos por las “nitrobacter”.
Pero de todas sus formas la más asimilable es el nitrógeno nítrico. Es la forma en la que la planta absorbe la mayor cantidad de nitrógeno. Es muy soluble en agua pero no es retenido por el poder absorbente del suelo, sino que desciende a capas profundas del terreno arrastrado por el agua. Durante este transporte es cuando las raíces deben tomarlo para no perderlo.
Si el nitrógeno aportado con los fertilizantes está en esta forma química, gran parte del mismo puede perderse al subsuelo sin que las raíces tengan tiempo para tomarlo. Esto provoca problemas muy graves de contaminación de aguas subterráneas que pueden llegar a ser consumidas en los hogares. Estudios científicos han desvelados que una elevada concentración de nitritos en el agua de consumo humano puede provocar determinados tipos de cáncer. Esto ha llevado a que en zonas especialmente sensibles como los deltas de ríos y lagunas las fertilizaciones nitrogenadas estén muy controladas. Para ello se recurre a la aportación de formulados donde el nitrógeno esté en forma orgánica lo que permite una menor lixiviación a las capas más profundas.

La carencia de nitrógeno se manifiesta por:
– un color verde claro en hojas jóvenes y amarillo pálido en las hojas más viejas, comenzando desde las puntas de las mismas hacia el interior. Luego caída de las hojas más viejas llegando a la desfoliación parcial o total de la planta
– se disminuye el crecimiento y la floración y se detiene la fructificación
Su exceso provoca:
– un desarrollo vegetativo desproporcionado con frutos de mala calidad, pequeños y en menor cantidad
– aumento de plagas puesto que es un atrayente para insectos chupadores como el pulgón o la mosca blanca
– acumulación de sustancias tóxicas en los tejidos
– carencia de otros nutrientes como el cobre ya que aumentan las necesidades de la planta por éste mineral.
Las formas químicas comerciales en las que podemos encontrar el nitrógeno son las siguientes:
– Amoniaco anhídrido: es el más rico en N y muy económico, pero es muy complejo su manejo puesto que se puede transformar en un gas fácilmente licuable, muy soluble en agua, que desprende gran cantidad de calor, irritante y muy explosivo.
– Amoniaco acuoso: es una solución acuosa concentrada de amoniaco anhídrido que pueden emplear únicamente los formuladores. Contiene un 20% de nitrógeno. Es más simple su manejo pero no está recomendado para personas con pocos conocimientos en química.
– Sulfato amónico: se comercializan en forma de cristales y presenta problemas de solidificación una vez ensacado.
– Nitrato amónico: es blanco, cristalino y muy soluble en agua. Su contenido en nitrógeno es del 35%. Puede explosionar por impacto o por calor.
– Nitrato sódico: también conocido como “caliche”. Es una mezcla natural proveniente de minas chilenas de proporciones más o menos variables de nitrato potásico, cloruros y sulfatos sódicos, cálcicos y magnésicos, junto con pequeñas cantidades de yodatos y boratos. Es un producto granulado que contiene un 16% de N y es muy soluble en agua. También se puede obtener industrialmente.
– Nitrato potásico: su coste es muy elevado puesto que sólo existen pequeños yacimientos en Índia, China o Egipto y no todos contienen los mismos niveles de pureza. Es estable y no explosivo, pero es un oxidante fuerte y acelera la descomposición de la materia orgánica. Interesante como fertilizante porque contiene nitrógeno y potasio en forma soluble.
– Nitrato cálcico: se produce en grandes cantidades en Europa, principalmente en Noruega y Alemania. Muy interesante por su contenido en calcio y muy favorable para muchos suelos con exceso de salinidad o pH elevados, pero tiene un contenido en nitrógeno relativamente bajo y propiedades físicas desfavorables. Debe guardarse en recipientes protegidos contra la humedad y debe aplicarse inmediatamente después de abrir los envases porque se pueden degradar muy fácilmente.
– Urea: es uno de los fertilizantes de mayor concentración en nitrógeno (en torno al 45%). Su consumo ha crecido mucho debido a su bajo coste y por no ser explosivo. Se comercializa tanto cristalizada o como granulada. Tiene el grave inconveniente de que es muy negativo para la vida microbiana del suelo.
– Estiércol: se forma a partir de los excrementos sólidos y líquidos del ganado y de los materiales de las camas de las cuadras, establos, etc… Estos materiales una vez recogidos se colocan en montones y se dejan fermentar durante periodos de tiempo que en función de las condiciones climáticas pueden ir de los tres a los seis meses. Contiene en torno al 1% de nitrógeno.
– Compost: es una de las consecuencias de la fermentación de los estiércoles, aunque también se pueden obtener de la fermentación aerobia de basuras y restos vegetales. De ésta forma se pueden obtener riquezas de nitrógeno de hasta el 4% porque en el proceso pueden perder más de un 50% de agua. La fermentación se controla por la adición de organismos microbianos, lombrices o por la inyección de aire.
Las formas comerciales más habituales suelen ser:
Liberación lenta: se presentan en forma de gránulos envueltos en una membrana semipermeable que está constituida por una sustancia insoluble o de baja solubilidad en agua. La disolución del fertilizante se produce lentamente conforme el agua va atravesando el recubrimiento. La membrana se va rompiendo y liberando los nutrientes de forma progresiva. Las sustancias más empleadas como recubrimiento son: azufre, resinas, caucho, parafinas, plástico perforado, etc… No son necesarias grandes concentraciones de humedad en el suelo.
Abonos de baja solubilidad: son abonos que requieren una gran cantidad de agua para su completa disolución. Aparecen en forma de polvo a distintas granulometrías y sus riquezas en nitrógeno y su pureza es baja.
Abonos con inhibidores de la nitrificación: las principales pérdidas de nitrógeno se producen después de su conversión a nitratos. Existen ciertos materiales que son tóxicos para las bacterias nitrificantes y cuando se añaden al suelo, pueden inhibir temporalmente la nitrificación. Por tanto, reducen las pérdidas de nitratos por lixiviación y desnitrificación y con ello se aumenta el rendimiento de los fertilizantes. La inhibición no debe ser total y estos productos deben ser selectivos, de forma que sólo actúen sobre los microorganismos nitrificantes, y no sobre otros microorganismos de las plantas. Estos productos resultan muy efectivos en suelos arenosos, para evitar el lavado de los nitratos y en suelos encharcados, para evitar la desnitrificación. Son productos derivados de la pirina y la pirimidina. Su persistencia en el suelo es de 2 a 3 meses y se elimina por volatilización y degradación a otros compuestos. Dicha persistencia depende fundamentalmente de tres factores:
– Textura del suelo: al aumentar el tamaño de las partículas, disminuye la persistencia del producto.
– Contenido de materia orgánica: el producto queda retenido en la materia orgánica.
– Temperatura del suelo: al aumentar la temperatura, disminuye la persistencia del producto, ya que aumenta su velocidad de degradación.
Acerca del autor
Muchos años luchando en la sombra para que el cannabis florezca al sol.





















